长期误诊的肉芽肿性皮肤松弛症一例
主诉 病史
患者男,40岁,农民。因左臀部皮下肿块及溃疡5年伴疼痛,皱褶部位皮肤松弛1年余,于2009年7月来我科就诊。患者5年前无明显诱因于左臀部出现一皮下包块,表面皮肤无明显变化,亦无症状。后于当地医院手术切除,病理检查示“肉芽肿性炎症”。术后伤口愈合良好。术后10天左右因参加防洪抢险,左侧臀部手术切口裂开,此后伤口处出现溃疡、脓性分泌物,溃疡进行性扩大,迁延不愈。患者在当地多家医院诊治,曾取皮肤病理拟诊为“皮肤深部真菌病”,口服伊曲康唑200mg/d及特比萘芬250mg/d半年及某些抗生素治疗(具体不详),皮损未见好转。1年余前患者左侧腹股沟处皮肤逐渐出现多发斑块,不久皮肤开始松弛并伴有褐色色素沉着,此后皮损渐进展至右侧腹股沟、腰腹部、双腋下及颈部,患者无明显自觉症状。起病以来,患者饮食尚可,睡眠欠佳,5年来体重下降10千克。既往史:2008年发现“直肠癌”,后行手术切除肿瘤,术后予CFA方案化疗2次,后因“肠梗阻”而终止化疗。个人史及家族史无特殊。
查体 辅查
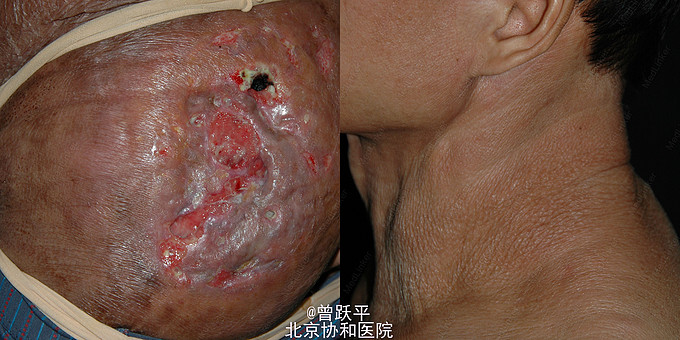
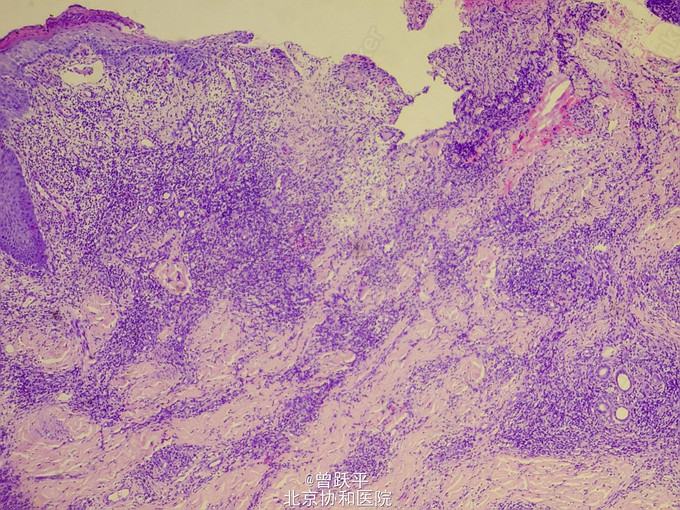
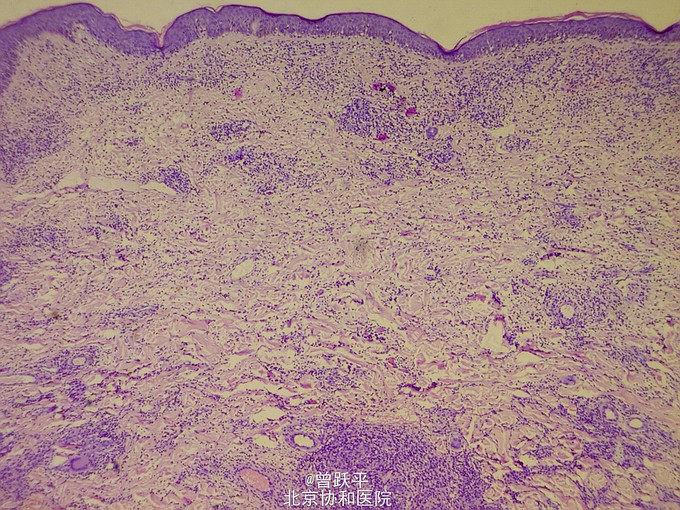
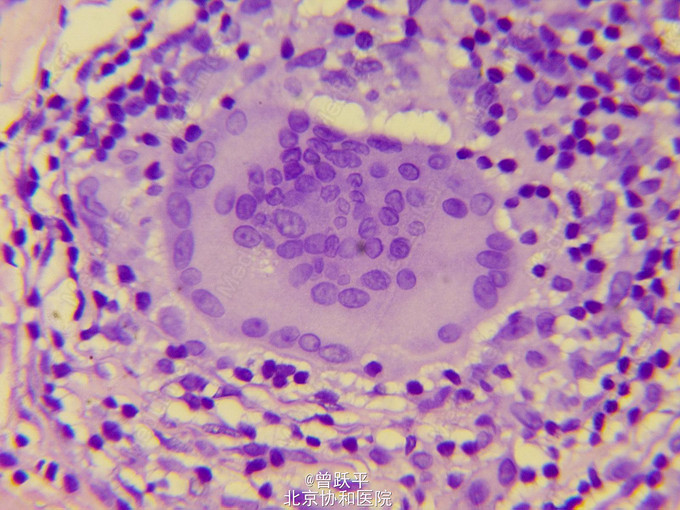
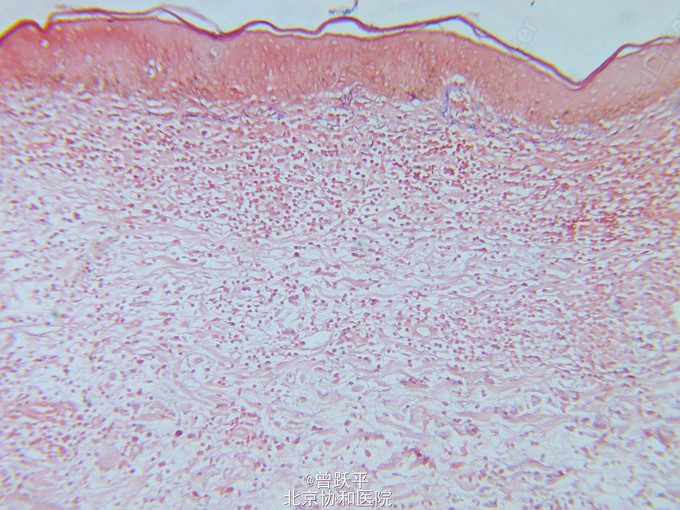
体格检查:慢性病容,精神差,消瘦,双腋下、双腹股沟可及多个黄豆至蚕豆大小肿大淋巴结,质韧,活动度差,无触痛。心肺查体未见明显异常。左下腹可见人造肛。全腹部无压痛,无腹胀。皮肤科情况:左臀部弥漫性暗红色斑块,其内多个大小不一深在性溃疡,有少许淡绿色脓性分泌物。斑块周围皮肤、颈部两侧、双腋下、腰背部、腹部、双侧腹股沟皮肤明显松弛、褶皱增多,皮肤表面萎缩、干燥。双大腿皮肤呈皮肤异色样改变。 实验室及辅助检查:血常规白细胞6.22×109/L,中性粒细胞百分比71%, 淋巴细胞百分比11.9%↓, 单核细胞百分比8.3%↑, 嗜酸性细胞百分比6.9%↑,红细胞4.45×1012/L,血红蛋白110 g/L↓, 血小板292×109/L。尿常规白细胞 125cells/μl↑,蛋白质 0.3g/L↑,红细胞 200cells/μl↑;肝肾功能示白蛋白 27g/L↓,肌酐196μmol/L↑,尿素氮 7.34mmol/L↑。淋巴细胞亚群分析示CD3+T% 57.8%↓,CD4+T% 26.8%↓,B% 33.2%↑。乙型肝炎病毒表面抗原(HbsAg)、丙型肝炎病毒抗体(HCV-Ab)、人类免疫缺陷病毒抗体(HIV-Ab)、梅毒快速血浆反应素试验(RPR)均阴性。免疫固定电泳未见单克隆蛋白。抗核抗体(ANA)、抗双链DNA抗体(dsDNA)、抗中性粒细胞胞浆抗体(ANCA)均阴性。脓性分泌物涂片抗酸染色阴性;脓性分泌物奴卡菌培养阴性,真菌培养阴性,铜绿假单孢菌(+++)。胸部CT平扫示右肺上叶后段结节钙化灶;右肺斑片、索条影,双肺小结节;双侧腋窝多发肿大淋巴结,皮下脂肪间隙模糊密度增高。腹部CT平扫示双肾结石,左侧肾盂扩张;右肾低密度影;脾大;腹膜后多发小结节影;直肠形态不规则;盆腔静脉石可能;双侧腹股沟多发肿大淋巴结;皮下脂肪密度弥漫性增高,左侧臀部软组织肿胀。双肾B超示双肾弥漫性病变,双肾多发结石,右肾囊肿,左肾积水。 组织病理检查: 1.(左臀部溃疡):角化不全,浅表溃疡,真皮浅层水肿,真皮内可见大量淋巴细胞、多核巨细胞浸润,多核巨细胞所含胞核多至40个,尚可见中等量的浆细胞及少量嗜酸性粒细胞浸润,真皮深层大片坏死。PAS染色阴性,抗酸染色阴性。弹力纤维染色示皮损处弹力纤维断裂、缺失。 2.(左颈部松弛处皮肤):表皮萎缩,基底细胞液化变性,可见单一核细胞移入表皮。真皮全层可见淋巴细胞、组织细胞弥漫性浸润,尚可见较多多核巨细胞,多核巨细胞所含胞核多至40个。弹力纤维染色示皮损处弹力纤维基本缺失。免疫组化示CD3(+),CD45RO(+++),CD43(+++),CD68(+),CD20(-),CD79α(-)。 3.(左臀部皮下包块,外院病理片):真皮至肌肉组织弥漫性淋巴细胞、组织细胞浸润,淋巴细胞核染色深,具有异型性,可见较多多核巨细胞,多核巨细胞核为10个左右。
诊断 处理
肉芽肿性皮肤松弛症
随访 讨论
肉芽肿性皮肤松弛症(granulomatous slack skin,GSS)平均发病年龄为37岁, 男女比例为2.9∶1。本病发病初期临床表现为非特异性,皮损多数为浸润性斑块,也可表现为丘疹、结节、限局性鳞屑斑,以及淡红色、紫红色斑片,也可出现溃疡。GSS一般无自觉症状,也可伴轻度瘙痒甚至剧痒。本病好发部位多为褶皱处,如腋窝、腹股沟,也可仅累及腹部、下肢、上肢等。本病慢性迁延,常在患者发病数年后出现皮肤松弛,表现为皮肤弹性降低、起皱、悬垂及萎缩,皮肤松弛可局限于某一部位,也可泛发全身。GSS皮肤以外其它系统受累的情况少见,但也有累及淋巴结、肺脏和脾脏的报道。 本例患者临床经过特殊之处在于其首先以皮下肿块起病,局部切除肿块后形成迁延不愈的皮肤溃疡,5年后全身以皱褶部位为主逐渐出现斑块,并发展至典型的皮肤松弛表现,左臀部溃疡周围皮肤亦出现松弛、褶皱增多的表现,最终取皮肤病理而明确诊断。患者全身及CT检查时提示双侧腋窝、腹股沟及腹膜后均有肿大淋巴结伴脾大,提示GSS可能已经累及淋巴结和脾脏,但患者拒绝行进一步检查,故尚不能明确患者皮肤外系统受累情况。 本病早期组织病理上表现为真皮上层小到中等程度大的淋巴细胞呈带状浸润, 有亲表皮性, 真皮乳头层和网状层弹性纤维均消失, 有含多达40个胞核的多核巨细胞及非干酪样肉芽肿存在。最显著的组织学特征为单一核细胞围绕多核巨细胞呈“花环状”排列。Verhoeff-van Gieson染色示弹力纤维缺失;进展期从真皮全层到部分皮下可见弥漫性淋巴样细胞浸润, 以及异物巨细胞和肉芽肿反应, 也可见嗜酸性粒细胞、B 淋巴细胞和浆细胞, 没有明显的表皮萎缩。免疫组化显示浸润的淋巴细胞主要为CD4+ CD45RO+ T细胞,也有CD30 阳性以及T细胞表面标记(CD3, CD5, and CD7) 阴性的报道。多核巨细胞表达CD14和CD68证实其来源于巨噬/单核细胞。本例患者左颈部皮肤松弛处组织病理改变为单一核细胞移入表皮,真皮全层可见淋巴细胞、组织细胞弥漫性浸润,尚可见较多多核巨细胞,弹力纤维染色示弹力纤维缺失。免疫组化结果示淋巴细胞CD3(+),CD43(+++),CD45RO(+++),CD20 和CD79α均阴性,提示肿瘤来源于T淋巴细胞,此外多核巨细胞CD68(+),提示其来源于巨噬/单核细胞。根据患者的临床表现、特征性的组织病理及免疫组化检查,GSS诊断成立。 患者长期误诊的重要原因为左臀部迁延不愈的溃疡,溃疡周围皮肤有松弛、褶皱增多的表现,组织病理与左颈部松弛处皮肤相似,符合GSS表现,故左臀部溃疡及其周围皮损处应为GSS累及所致。患者既往左臀部有手术史及可疑感染史,迁延不愈溃疡的原因应注意除外慢性感染性疾病如深部真菌病和非典型分枝杆菌感染等可能,但患者长期抗感染治疗无效,用感染性疾病不能完全解释。可能的解释为患者当时切除皮下肿块后,由于GSS累及该部位,其真皮内弹力纤维断裂、缺失,皮肤张力不足,导致术后伤口容易崩裂,在GSS皮损的基础上继发感染,因而形成慢性迁延不愈的溃疡。我们进一步复习患者5年前外院切取的皮下肿块病理,发现其真皮至肌肉组织有弥漫性淋巴细胞、组织细胞浸润,淋巴细胞核染色深,具有异型性,可见较多多核巨细胞,多核巨细胞核为10个左右,可见当时患者已有GSS的组织病理表现。由于本病罕见,且患者初发皮损表现不特异,故当时病理仅报告“肉芽肿性炎”,而未行进一步免疫组化染色等检查,导致患者长期无法确诊。因此提高临床医生对本病临床及组织病理特点的认识,对早期诊断大有帮助。 根据患者左臀部溃疡的临床表现及组织病理特点,鉴别诊断还应包括转移性克隆(Crohn)氏病和溃疡性肉芽肿性蕈样肉芽肿。转移性克隆(Crohn)氏病患者肛周、外阴、臀部皮肤可出现溃疡性病变,组织病理显示真皮全层非化脓性结节病样肉芽肿改变。但患者往往具有克隆(Crohn)氏病的肠道表现,不难鉴别。溃疡性肉芽肿性蕈样肉芽肿(GMF):GSS与GMF的组织病理表现及免疫表型相似,但GSS的多核巨细胞较GMF的体积更大,含有的胞核也更多。GSS的每个多核巨细胞可含有多至40个核,而GMF的一般仅含5至10个核。本例患者的每个多核巨细胞含有多至40个核,结合皮损处弹力纤维染色示弹力纤维基本缺失以及皱褶部位典型临床表现,GSS诊断明确。 临床上约一半的患者在皮肤内或皮肤外伴发其它淋巴细胞增生性疾病,如霍奇金淋巴瘤(约1/3的患者伴发)、非霍奇金淋巴瘤、蕈样肉芽肿、急性髓性白血病和朗格汉斯细胞组织增生症。本例患者未发现其它恶性淋巴细胞增生性疾病伴发证据,但他在起病4年后伴发“直肠癌”(经手术切除,病理证实),目前尚无GSS与直肠癌并发的报道。GSS与直肠癌并发是某种巧合,抑或存在某种内在的联系,现在仍不清楚。
